Eine verhängnisvolle Affäre
Krebszellen gehen mit Blutgefäßen eine unglückselige Liaison ein – eine Beziehung, die sich therapeutisch nutzen lässt
von Andreas Fischer und Hellmut Augustin
Trotz erheblicher Fortschritte in Prävention und Therapie sind Krebsleiden nach den Herz-Kreislauferkrankungen weiterhin die zweithäufigste Todesursache in der westlichen Welt. In der Gruppe der unter 75-Jährigen haben Tumorerkrankungen mittlerweile die Herz-Kreislauferkrankungen als Todesursache Nummer 1 abgelöst. Die seit langem etablierten Behandlungsmethoden der Chirurgie, Strahlen- und Chemotherapie werden seit wenigen Jahren ergänzt durch Substanzen, die gezielt Tumorzellen bekämpfen, ohne dabei gesunde Zellen zu schädigen.
Ein weiteres Konzept zur Krebsbekämpfung wurde bereits vor rund 40 Jahren von Judah Folkman vom Children’s Hospital in Boston vorgeschlagen. Der amerikanische Chirurg und Wissenschafter erkannte, dass Tumoren aktiv das Einwachsen von Blutgefäßen bewirken. Würde dieses Gefäßwachstum unterbunden, so die Überlegungen Folkmans, könnte man den Tumor von seiner Versorgung abschneiden, ihn gleichsam aushungern und auf diese Weise sein weiteres Wachstum sowie die Metastasierung – das Entstehen gefährlicher Tochtergeschwülste – verhindern.
von Andreas Fischer und Hellmut Augustin
Das über Jahrzehnte angezweifelte Konzept der Tumor-Anti-Angiogenese – dem Bekämpfen von Tumoren mit Medikamenten, die das überschießende Wachstum von Blutgefäßen in bösartigen Geschwülste unterbinden – hat sich mittlerweile als zusätzlicher Baustein der Krebsbehandlung etabliert. Ein noch besseres Verständnis der Neubildung von Gefäßen lässt auf weitere neue Therapieansätze hoffen – nicht nur, um Krebs zu behandeln, sondern auch um Herzinfarkte oder Schlaganfälle zu verhindern.
Trotz erheblicher Fortschritte in Prävention und Therapie sind Krebsleiden nach den Herz-Kreislauferkrankungen weiterhin die zweithäufigste Todesursache in der westlichen Welt. In der Gruppe der unter 75-Jährigen haben Tumorerkrankungen mittlerweile die Herz-Kreislauferkrankungen als Todesursache Nummer 1 abgelöst. Die seit langem etablierten Behandlungsmethoden der Chirurgie, Strahlen- und Chemotherapie werden seit wenigen Jahren ergänzt durch Substanzen, die gezielt Tumorzellen bekämpfen, ohne dabei gesunde Zellen zu schädigen.
Ein weiteres Konzept zur Krebsbekämpfung wurde bereits vor rund 40 Jahren von Judah Folkman vom Children’s Hospital in Boston vorgeschlagen. Der amerikanische Chirurg und Wissenschafter erkannte, dass Tumoren aktiv das Einwachsen von Blutgefäßen bewirken. Würde dieses Gefäßwachstum unterbunden, so die Überlegungen Folkmans, könnte man den Tumor von seiner Versorgung abschneiden, ihn gleichsam aushungern und auf diese Weise sein weiteres Wachstum sowie die Metastasierung – das Entstehen gefährlicher Tochtergeschwülste – verhindern.
 |
|
|
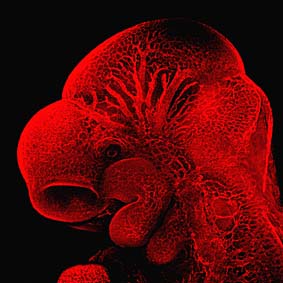
Im Detail: der Embryo einer Maus und seine Blutgefäße
|
Folkmans Hypothese von der „Anti-Angiogenese“ wurde über viele Jahre hinweg von der Fachwelt kritisiert, fand aber spätestens Ende der 1980er Jahre mit der Entdeckung des blutgefäßspezifischen Wachstumsfaktors VEGF (vaskulärer endothelialer Wachstumsfaktor) große Beachtung. Es stellte sich heraus, dass Tumoren große Mengen von VEGF und anderen Wachstumsfaktoren bilden und dadurch die Neubildung von Blutgefäßen veranlassen. In den 90er Jahren ließ sich schließlich im Tiermodell bestätigen, dass sich das Tumorwachstum durch Substanzen, die VEGF hemmen, drastisch bremsen lässt. Seit kurzem steht ein erster VEGF-Hemmstoff (Bevacizumab) als Medikament zur Verfügung. Er wird mit herkömmlichen chemotherapeutischen Medikamenten kombiniert und zur Behandlung von Krebserkrankungen des Darms, von Niere, Brust und Lunge verwendet. Damit hat sich das Konzept der Anti-Angiogenese als weiterer Baustein der Krebsbehandlung durchgesetzt. Eine Reihe weiterer Wirkstoffe, die auch andere Wachstumsfaktoren, ihre Rezeptoren oder nachgeschaltete Signalwege blockieren, werden derzeit klinisch geprüft.
Der gemeinsame Forschungsbereich „Vaskuläre Biologie und Tumorangiogenese“ des Zentrums für Biomedizin und Medizintechnik in Mannheim und des Deutschen Krebsforschungszentrum in Heidelberg hat sich die Aufgabe gestellt, das Konzept der Anti-Angiogenese weiter zu verbessern und mehr darüber zu erfahren, wie das von Tumoren initiierte Wachstum von Blutgefäßen und die Metastasierung gesteuert werden und wie dem entgegengewirkt werden kann. Eine grundsätzliche Frage, die es dabei bis ins molekulare Detail zu klären gilt, ist, was während der Angiogenese geschieht, wie also Blutgefäße natürlicherweise im Körper entstehen.
Bereits der frühe Embryo verfügt über ein funktionierendes Herz-Kreislaufsystem, damit die mütterlichen Nährstoffe im heranwachsenden Organismus verteilt werden können. Das Gefäßsystem entsteht, indem sich einzelne Zellen, sogenannte Endothelzellen, zu winzigen Röhren zusammenlagern. Aus diesen Röhrchen sprossen weitere Endothelzellen aus, sie teilen sich weiter und bilden erneut ein Röhrchen. Doch auch damit ist noch kein fertiges Blutgefäß entstanden. Zahlreiche Umbauprozesse schließen sich an, glatte Muskelzellen und anderen Gefäßwandzellen werden rekrutiert und stabilisieren die Röhrchen von außen. Das Ergebnis ist letztendlich ein geordnetes Gefäßsystem mit Arterien, die Blut vom Herzen zu den Organen leiten, und Venen, die für den Rücktransport verantwortlich sind. Zwischengeschaltet sind Kapillaren, sehr dünne Gefäße, die den Stoff- und Gasaustausch zwischen Blut und Gewebe ermöglichen.
Nicht nur im Embryo, auch im ausgewachsenen Organismus findet Angiogenese statt. Bei der Wundheilung oder beim Muskelwachstum entstehen neue Gefäße; auch während des weiblichen Menstruationszyklus und zur Bildung der Plazenta in der Schwangerschaft sind Angiogenese-Vorgänge unerlässlich. Die Gefäßbildung ist ein für alle Stadien des Lebens unentbehrlicher Vorgang.
Der gemeinsame Forschungsbereich „Vaskuläre Biologie und Tumorangiogenese“ des Zentrums für Biomedizin und Medizintechnik in Mannheim und des Deutschen Krebsforschungszentrum in Heidelberg hat sich die Aufgabe gestellt, das Konzept der Anti-Angiogenese weiter zu verbessern und mehr darüber zu erfahren, wie das von Tumoren initiierte Wachstum von Blutgefäßen und die Metastasierung gesteuert werden und wie dem entgegengewirkt werden kann. Eine grundsätzliche Frage, die es dabei bis ins molekulare Detail zu klären gilt, ist, was während der Angiogenese geschieht, wie also Blutgefäße natürlicherweise im Körper entstehen.
Bereits der frühe Embryo verfügt über ein funktionierendes Herz-Kreislaufsystem, damit die mütterlichen Nährstoffe im heranwachsenden Organismus verteilt werden können. Das Gefäßsystem entsteht, indem sich einzelne Zellen, sogenannte Endothelzellen, zu winzigen Röhren zusammenlagern. Aus diesen Röhrchen sprossen weitere Endothelzellen aus, sie teilen sich weiter und bilden erneut ein Röhrchen. Doch auch damit ist noch kein fertiges Blutgefäß entstanden. Zahlreiche Umbauprozesse schließen sich an, glatte Muskelzellen und anderen Gefäßwandzellen werden rekrutiert und stabilisieren die Röhrchen von außen. Das Ergebnis ist letztendlich ein geordnetes Gefäßsystem mit Arterien, die Blut vom Herzen zu den Organen leiten, und Venen, die für den Rücktransport verantwortlich sind. Zwischengeschaltet sind Kapillaren, sehr dünne Gefäße, die den Stoff- und Gasaustausch zwischen Blut und Gewebe ermöglichen.
Nicht nur im Embryo, auch im ausgewachsenen Organismus findet Angiogenese statt. Bei der Wundheilung oder beim Muskelwachstum entstehen neue Gefäße; auch während des weiblichen Menstruationszyklus und zur Bildung der Plazenta in der Schwangerschaft sind Angiogenese-Vorgänge unerlässlich. Die Gefäßbildung ist ein für alle Stadien des Lebens unentbehrlicher Vorgang.
 |
|
|
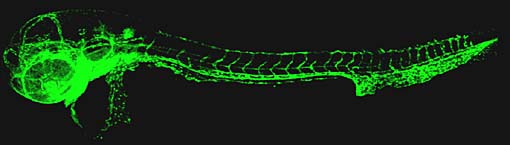
Der Embryo eines Zebrafisches, zwei Tage nach der Befruchtung: Die genetisch veränderten Tiere produzieren ein grün fluoreszierendes Protein ausschließlich in den Endothelzellen der Blutgefäße. Die Wissenschaftler können das Wachstum der Blutgefäße auf diese Weise über lange Zeit hinweg mithilfe eines Fluoreszenzmikroskops studieren.
|
Ein fehlgeleitetes Blutgefäßwachstum indes trägt zum Fortschreiten etlicher Krankheiten bei. Ein Tumor etwa kann ohne Blutgefäß-Neubildung nicht größer als etwa ein Millimeter werden. Ab dann ist eine Versorgung der Krebszellen ausschließlich über Diffusion, den einfachen Stoffaustausch, nicht mehr möglich. Vor allem das Zentrum des herangewachsenen Zellhaufens wird dann nicht mehr ausreichend mit Sauerstoff versorgt. Der Sauerstoffmangel (Hypoxie) bewirkt, dass die Zellen ein Notprogramm anschalten und ihren Stoffwechsel auf Milchsäuregärung umstellen, die ohne Sauerstoff erfolgen kann. Darüber hinaus werden zahlreiche Botenstoffe, darunter VEGF, freigesetzt, die Blutgefäße dazu anregen, aus benachbarten Geweben in Richtung Tumorzellen zu wachsen. Haben sie Anschluss gefunden, ist die Sauerstoff- und Nährstoffversorgung der entarteten Zellen gewährleistet, sie überleben, können sich weiter teilen und zu einer gefährlichen Geschwulst heranwachsen.
Bei manchen Augenerkrankungen, etwa der feuchten Makuladegeneration, ist eine übermäßig starke Neubildung von Blutgefäßen in der Netzhaut verantwortlich für den Verlust der Sehkraft. Auch hier sind es Sauerstoffmangelzustände, die zunächst das massive Entstehen neuer Gefäße veranlassen. Da die Gefäße aber häufig sehr fragil sind, kommt es wiederholt zu Einblutungen im Auge, was das Fortschreiten der Erkrankung bis hin zur Erblindung begünstigt. Die feuchte Makuladegeneration ist nicht selten, sie gehört zu den häufigsten Ursachen für Sehverlust und Blindheit bei Menschen über 65 Jahren in Europa und den Vereinigten Staaten.
Schließlich sind auch bei manchen chronischen Entzündungen und Hauterkrankungen wie der Schuppenflechte (Psoriasis) angiogene Sprossungen für einen fortschreitenden Krankheitsverlauf mitverantwortlich. Bei der Psoriasis etwa setzen Abwehrzellen Botenstoffe frei, welche die Gefäßneubildung anregen. Sie wachsen in Regionen der Haut ein, die normalerweise frei von Gefäßen sind. Dies bedingt, dass noch mehr Abwehrzellen in die Hautregion einwandern und den Entzündungsprozess verstärken.
Bei manchen Augenerkrankungen, etwa der feuchten Makuladegeneration, ist eine übermäßig starke Neubildung von Blutgefäßen in der Netzhaut verantwortlich für den Verlust der Sehkraft. Auch hier sind es Sauerstoffmangelzustände, die zunächst das massive Entstehen neuer Gefäße veranlassen. Da die Gefäße aber häufig sehr fragil sind, kommt es wiederholt zu Einblutungen im Auge, was das Fortschreiten der Erkrankung bis hin zur Erblindung begünstigt. Die feuchte Makuladegeneration ist nicht selten, sie gehört zu den häufigsten Ursachen für Sehverlust und Blindheit bei Menschen über 65 Jahren in Europa und den Vereinigten Staaten.
Schließlich sind auch bei manchen chronischen Entzündungen und Hauterkrankungen wie der Schuppenflechte (Psoriasis) angiogene Sprossungen für einen fortschreitenden Krankheitsverlauf mitverantwortlich. Bei der Psoriasis etwa setzen Abwehrzellen Botenstoffe frei, welche die Gefäßneubildung anregen. Sie wachsen in Regionen der Haut ein, die normalerweise frei von Gefäßen sind. Dies bedingt, dass noch mehr Abwehrzellen in die Hautregion einwandern und den Entzündungsprozess verstärken.
Die Hypothese, dass das Wachstum von Tumoren reduziert werden kann, wenn man ihre Nahrungszufuhr kappt, gilt inzwischen als gesichert. Zurzeit beschränkt sich diese Therapie noch auf die Hemmung des Wachstumsfaktors VEGF in Kombination mit klassischen Chemotherapeutika. Problematisch sind hierbei zumindest zwei Beobachtungen: Erstens können die VEGF-Hemmstoffe nicht alle Tumorgefäße zerstören; es reifen vielmehr einige der übrig gebliebenen Gefäße aus und lassen sich mit den bisher zugelassenen Hemmstoffen nicht mehr beeinflussen. Dieser Vorgang wird als „Normalisierung“ beschrieben. Zweitens entwickeln zahlreiche Tumoren Resistenzen gegen die VEGF-Blockade, indem sie das Gefäßwachstum über andere Wachstumsfaktoren stimulieren.
Große Erfolge erzielen VEGF-Hemmstoffe bei der Behandlung der feuchten Makuladegeneration. Die wiederholte lokale Verabreichung reduziert die überschüssige Blutgefäßbildung, und die weitere Neubildung von Gefäßen wird gestoppt. Hier ermöglicht es die anti-angiogene Therapie, viele Patienten vor der Erblindung zu bewahren.
Die Grundlagenforschung hat mittlerweile zahlreiche weitere molekulare Faktoren erkannt, welche die Angiogenese steuern. Dieses Wissen erlaubt nun erstmals klinische Versuche mit „pro-angiogenen“ Therapien. Dieses neue Konzept ist von großer medizinischer Bedeutung. Denn eine nicht ausreichende Blutversorgung führt zu so häufigen Erkrankungen wie Herzinfarkt, Schlaganfall oder zur peripheren arteriellen Verschlusskrankheit. Das Ziel pro-angiogener Strategien ist, das Programm zur Blutgefäßneubildung in bedrohlich verengten Gefäßen zu starten, damit sich Umgehungskreisläufe bilden können, welche die Versorgung mit Blut aufrechterhalten. Auf diese Weise kann verhindert werden, dass unterversorgtes Gewebe abstirbt. Zahlreiche Versuchsansätze mit VEGF und anderen Wachstumsfaktoren für eine Pro-Angiogenese werden derzeit erprobt.
Mit dem gemeinsamen Forschungsbereich „Vaskuläre Biologie und Tumorangiogenese“ wurde in der Region Heidelberg-Mannheim einer der größten Schwerpunkte gefäßbiologischer Forschung in Deutschland geschaffen. Wir untersuchen in unserem Forschungsbereich verschiedene Aspekte der Gefäßbildung und des Tumorwachstums. Ein Schwerpunkt ist die Frage, wie das gerichtete Aussprossen neuer Gefäße durch unterschiedliche Wachstumsfaktoren und deren Andockstationen (Rezeptoren) auf der Oberfläche der Endothelzellen bestimmt wird. Dabei konnte gezeigt werden, dass zahlreiche der daran beteiligten Moleküle (Ephrine, Semaphorine, Neuropiline, Delta-Notch) nicht nur das Auswachsen von Blutgefäßen, sondern auch das gerichtete Wachstum von Nervenzellen steuern. Offensichtlich wird der evolutionär erfolgreiche Mechanismus von verschiedenen biologischen Systemen genutzt.
Große Erfolge erzielen VEGF-Hemmstoffe bei der Behandlung der feuchten Makuladegeneration. Die wiederholte lokale Verabreichung reduziert die überschüssige Blutgefäßbildung, und die weitere Neubildung von Gefäßen wird gestoppt. Hier ermöglicht es die anti-angiogene Therapie, viele Patienten vor der Erblindung zu bewahren.
Die Grundlagenforschung hat mittlerweile zahlreiche weitere molekulare Faktoren erkannt, welche die Angiogenese steuern. Dieses Wissen erlaubt nun erstmals klinische Versuche mit „pro-angiogenen“ Therapien. Dieses neue Konzept ist von großer medizinischer Bedeutung. Denn eine nicht ausreichende Blutversorgung führt zu so häufigen Erkrankungen wie Herzinfarkt, Schlaganfall oder zur peripheren arteriellen Verschlusskrankheit. Das Ziel pro-angiogener Strategien ist, das Programm zur Blutgefäßneubildung in bedrohlich verengten Gefäßen zu starten, damit sich Umgehungskreisläufe bilden können, welche die Versorgung mit Blut aufrechterhalten. Auf diese Weise kann verhindert werden, dass unterversorgtes Gewebe abstirbt. Zahlreiche Versuchsansätze mit VEGF und anderen Wachstumsfaktoren für eine Pro-Angiogenese werden derzeit erprobt.
Mit dem gemeinsamen Forschungsbereich „Vaskuläre Biologie und Tumorangiogenese“ wurde in der Region Heidelberg-Mannheim einer der größten Schwerpunkte gefäßbiologischer Forschung in Deutschland geschaffen. Wir untersuchen in unserem Forschungsbereich verschiedene Aspekte der Gefäßbildung und des Tumorwachstums. Ein Schwerpunkt ist die Frage, wie das gerichtete Aussprossen neuer Gefäße durch unterschiedliche Wachstumsfaktoren und deren Andockstationen (Rezeptoren) auf der Oberfläche der Endothelzellen bestimmt wird. Dabei konnte gezeigt werden, dass zahlreiche der daran beteiligten Moleküle (Ephrine, Semaphorine, Neuropiline, Delta-Notch) nicht nur das Auswachsen von Blutgefäßen, sondern auch das gerichtete Wachstum von Nervenzellen steuern. Offensichtlich wird der evolutionär erfolgreiche Mechanismus von verschiedenen biologischen Systemen genutzt.
 |
|
|
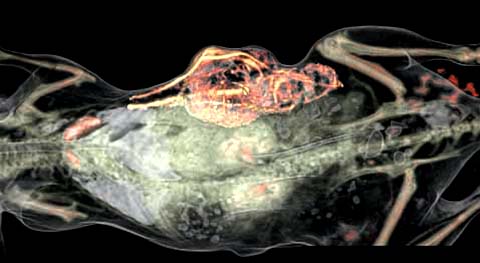
Klare Verhältnisse: Hochauflösende bildgebende Verfahren machen das Skelett und die inneren Organe im Körper einer Maus deutlich sichtbar. Ebenso deutlich zu erkennen ist der Tumor in der Flanke. Aufgrund der massiven Entwicklung neuer Blutgefäße (rot, gelb) wird die Geschwulst extrem gut mit Blut versorgt.
|
Unsere Arbeiten legen zudem den Schluss nahe, dass bestimmte Wachstumsfaktoren und ihre Andockstationen auf Endothelzellen (Ephrine und ihre Rezeptoren) von Tumorzellen gebraucht werden, um den Ort ihres Entstehens zu verlassen und sich als Metastasen in weit entfernten Körperregionen abzusiedeln. Diese Erkenntnis könnte ein erster wichtiger Ansatzpunkt sein, um das Ansiedeln von Tochtergeschwülsten zu verhindern.
Ein zweiter Schwerpunkt unserer Forschungsarbeiten ist zu verstehen, wie Blutgefäße ausreifen und wie sie auf Schädigungen reagieren. In diesem Zusammenhang interessieren wir uns besonders für das sogenannte Angiopoietin-System. Der Botenstoff Angiopoietin-1 stabilisiert das ruhende Gefäßendothel, das verwandte Angiopoetin-2 hingegen wird von Endothelzellen vor allem in Stresssituationen freigesetzt, etwa bei bakteriellen Infektionen. Angiopoetin-2 bewirkt, dass die Gefäßwand in kürzester Frist durchlässig wird, damit Abwehrzellen aus dem Blut in das betroffene Gewebe einwandern können. Dies ist notwendig, damit der Organismus die Infektionserreger erfolgreich bekämpfen kann. Da es während des Wachstums von Tumoren ebenfalls zu Entzündungen kommt, ist es wahrscheinlich, dass der Botenstoff Angiopoetin-2 auch beim Fortschreiten von Tumorerkrankungen eine wichtige Rolle spielt. Gegenwärtig untersuchen wir auf molekularer Ebene, wie Angiopoietin-2 das Tumorwachstum und die Metastasierung steuert.
Der dritte Schwerpunkt unserer Forschungsarbeiten ist die Analyse des Bindegewebes (Stroma), das den Tumor umgibt, zu seinem Wachstum beiträgt und die Metastasierung begünstigt. Wir untersuchen hierzu Moleküle, die für das Stroma typisch sind, und wollen herausfinden, wie sie das Wachstum benachbarter Krebs- und Blutgefäßzellen beeinflussen. Aus therapeutischer Sicht erscheint es sehr attraktiv, das Stroma für einen medikamentösen Angriff auf den Tumor zu nutzen: Stroma-Bindegewebszellen sind normalerweise genetisch stabil; es ist daher nicht zu erwarten, dass sie während der Therapie Resistenzen entwickeln, wie es häufig bei Tumorzellen der Fall ist.
Ein zweiter Schwerpunkt unserer Forschungsarbeiten ist zu verstehen, wie Blutgefäße ausreifen und wie sie auf Schädigungen reagieren. In diesem Zusammenhang interessieren wir uns besonders für das sogenannte Angiopoietin-System. Der Botenstoff Angiopoietin-1 stabilisiert das ruhende Gefäßendothel, das verwandte Angiopoetin-2 hingegen wird von Endothelzellen vor allem in Stresssituationen freigesetzt, etwa bei bakteriellen Infektionen. Angiopoetin-2 bewirkt, dass die Gefäßwand in kürzester Frist durchlässig wird, damit Abwehrzellen aus dem Blut in das betroffene Gewebe einwandern können. Dies ist notwendig, damit der Organismus die Infektionserreger erfolgreich bekämpfen kann. Da es während des Wachstums von Tumoren ebenfalls zu Entzündungen kommt, ist es wahrscheinlich, dass der Botenstoff Angiopoetin-2 auch beim Fortschreiten von Tumorerkrankungen eine wichtige Rolle spielt. Gegenwärtig untersuchen wir auf molekularer Ebene, wie Angiopoietin-2 das Tumorwachstum und die Metastasierung steuert.
Der dritte Schwerpunkt unserer Forschungsarbeiten ist die Analyse des Bindegewebes (Stroma), das den Tumor umgibt, zu seinem Wachstum beiträgt und die Metastasierung begünstigt. Wir untersuchen hierzu Moleküle, die für das Stroma typisch sind, und wollen herausfinden, wie sie das Wachstum benachbarter Krebs- und Blutgefäßzellen beeinflussen. Aus therapeutischer Sicht erscheint es sehr attraktiv, das Stroma für einen medikamentösen Angriff auf den Tumor zu nutzen: Stroma-Bindegewebszellen sind normalerweise genetisch stabil; es ist daher nicht zu erwarten, dass sie während der Therapie Resistenzen entwickeln, wie es häufig bei Tumorzellen der Fall ist.
 |
|
|
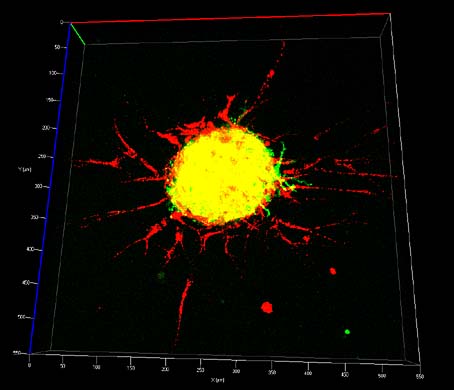
Isolierte Gefäßwandzellen lagern sich unter bestimmten Bedingungen in der Zellkultur spontan zu „Sphäroiden“ zusammen. Das oben abgebildete Sphäroid besteht aus rot und grün gefärbten Zellen. Einige der rot markierten Zellen sind ausgewandert und haben erste primitive Blutgefäße gebildet.
|
Eines der wichtigsten Hindernisse auf dem Weg zur eingehenden Analyse des Tumorstromas und seiner möglichen therapeutischen Beeinflussung war bislang, dass ein geeignetes Tiermodell für die Untersuchungen fehlte. Nicht nur in dieser, auch in vielerlei anderer Hinsicht stellen die derzeit benutzten Maus-Tiermodelle menschliche Krebserkrankungen nur unzureichend dar. Dringend erforderlich sind neue Tumormodelle, die es stellvertretend ermöglichen, menschliche Tumorerkrankungen zu erforschen, neue Wirkstoffe zu entwickeln und in Untersuchungen mit Tieren zu testen.
Wir haben kürzlich ein neues Verfahren entwickelt, mit dem sich ein komplexes menschliches Blutgefäßsystem in der Maus erzeugen lässt. Das Verfahren basiert auf der Beobachtung, dass sich isolierte Gefäßwandzellen unter bestimmten Bedingungen in der Zellkultur spontan zu Aggregaten, Sphäroiden, zusammenlagern. Diese Sphäroide können, in eine Gelmatrix eingebettet, unter die Haut von Mäusen gespritzt und mittels Wachstumsfaktoren zur Bildung eines Netzwerks menschlicher Blutgefäße angeregt werden. Anhand dieses Modells lässt sich nun untersuchen, wie Tumoren das Blutgefäßsystem beeinflussen. Es lassen sich darüber hinaus Wirkstoffe, die speziell gegen menschliche Proteine gerichtet sind, für die Therapie testen. Wir hoffen, damit in den nächsten Jahren weitere grundlegende Mechanismen der Gefäßbiologie aufzuklären und Grundsteine für neue Medikamente gegen Tumoren und andere schwere Erkrankungen des Menschen legen zu können.
Wir haben kürzlich ein neues Verfahren entwickelt, mit dem sich ein komplexes menschliches Blutgefäßsystem in der Maus erzeugen lässt. Das Verfahren basiert auf der Beobachtung, dass sich isolierte Gefäßwandzellen unter bestimmten Bedingungen in der Zellkultur spontan zu Aggregaten, Sphäroiden, zusammenlagern. Diese Sphäroide können, in eine Gelmatrix eingebettet, unter die Haut von Mäusen gespritzt und mittels Wachstumsfaktoren zur Bildung eines Netzwerks menschlicher Blutgefäße angeregt werden. Anhand dieses Modells lässt sich nun untersuchen, wie Tumoren das Blutgefäßsystem beeinflussen. Es lassen sich darüber hinaus Wirkstoffe, die speziell gegen menschliche Proteine gerichtet sind, für die Therapie testen. Wir hoffen, damit in den nächsten Jahren weitere grundlegende Mechanismen der Gefäßbiologie aufzuklären und Grundsteine für neue Medikamente gegen Tumoren und andere schwere Erkrankungen des Menschen legen zu können.
 |
|
Prof. Dr. Hellmut Augustin (rechts) leitet seit dem Jahr 2006 die Abteilung „Vaskuläre Onkologie und Metastasierung“ im Deutschen Krebsforschungszentrum Heidelberg und ist Inhaber des Lehrstuhls „Vaskuläre Biologie und Tumorangiogenese“ der Medizinischen Fakultät Mannheim der Universität Heidelberg. Sein Forschungsschwerpunkt ist die Biologie der Blut- und Lymphgefäße, die Blutversorgung von Tumoren und die Metastasierung.
Kontakt: augustin@angiogenese.de
Dr. Andreas Fischer leitet seit dem Jahr 2007 eine unabhängige Forschergruppe im Forschungsbereich „Vaskuläre Biologie“. Seine Arbeitsgruppe ist auf dem Gebiet der entwicklungsbiologischen Angiogenese tätig.
Homepage: www.angiolab.de
Kontakt: augustin@angiogenese.de
Dr. Andreas Fischer leitet seit dem Jahr 2007 eine unabhängige Forschergruppe im Forschungsbereich „Vaskuläre Biologie“. Seine Arbeitsgruppe ist auf dem Gebiet der entwicklungsbiologischen Angiogenese tätig.
Homepage: www.angiolab.de
Seitenbearbeiter:
E-Mail
Letzte Änderung:
27.11.2014

